百济神州的业绩
2月27日,百济神州发布2025年业绩快报,报告期内,公司产品收入为377.70亿元,较上年同比上升39.9%,上年同期产品收入为269.94亿元,公司营业总收入为382.05亿元,较上年同比上升40.4%,公司归属于母公司所有者的净利润14.22亿元,首次实现全年盈利。此外,公司总资产574.23亿元,较期初增加34.1%,归属于母公司的所有者权益306.01亿元,较期初增加26.6%。
百悦泽(泽布替尼)依然是最大贡献
百济神州表示,业绩的增长主要由于百悦泽(泽布替尼,BTK抑制剂),以及安进公司授权产品(安加维 (地舒单抗)、KYPROLIS(卡非佐米)、BLINCYTO(倍林妥莫双抗),中国市场权益)和百泽安(替雷利珠单抗 PD-1)的销售增长。
其中百悦泽(泽布替尼,BTK抑制剂)贡献了大部分收入,2025年,百悦泽全球销售额总计280.67亿元,同比增长48.8%,约占营业总收入的73.4%,百泽安(替雷利珠单抗 PD-1)全球销售额总计52.97亿元,同比增长18.6%,约占营业总收入的13.9%。2025年,安进公司授权许可产品销售额为34.71亿元,同比增长33.6%,约占营业总收入的9%,三者合计约占百济神州2025年营业总收入的96.3%。
美国是其最主要市场
百济神州公告显示,百悦泽(泽布替尼,BTK抑制剂)临床开发项目迄今已在全球超过30个国家和地区开展超过45项试验,入组超过7900例患者,目前已在全球超过75个市场获批。百泽安(替雷利珠单抗 PD-1)临床开发项目迄今已在全球超过33个国家和地区入组超过15800例受试者,已在全球超过50个市场获批。
整体而言,百济神州上述两款药品全球拓展成果丰硕,但美国依然是最重要的收入来源,百济神州称,百悦泽(泽布替尼,BTK抑制剂)美国市场2025年销售额总计202.06亿元,同比增长45.5%,占百悦泽2025年营收的72%,占百济神州2025年全年总营收的53%。欧洲销售额总计42.65亿元,同比增长66.4%,占百悦泽2025年营收的15%,占百济神州2025年全年总营收的11%。中国市场销售额为24.72亿元,同比增长33.1%,占百悦泽2025年营收的8.8%,占百济神州2025年全年总营收的6.4%。
2026年预计营收人民币436亿元至450亿元之间,但增长放缓
同一天,百济神州还发布了2026年度经营业绩预测,这在A股市场上很少见,显示了百济神州对未来发展的信心,其预测,百济神州2026年全年营业收入预计将介于人民币436亿元至450亿元之间,这意味着相比2025年,百济神州2026年营收将增长14.1%-17.8%,虽然增幅依然上涨,但涨幅显然大幅低于2025年40.1%,此前,2024年涨幅为56.19%,2023年涨幅82.13%,意味着百济神州营收增长进入一定的瓶颈期。或许因为此原因,百济神州近几日股价连续下跌。
展望2026年,百济神州称与JazzPharmaceuticals和Zymeworks合作,公布了HERIZON-GEA-01试验的完整数据:与曲妥珠单抗联合化疗相比,百泽安(替雷利珠单抗 PD-1)联合百赫安(百济神州另一款产品,泽尼达妥单抗 双特异性HER2抑制剂,2024年以来,先后在美国、欧洲和中国获批上市,但从目前业绩看,营收还未显示出明显成绩)与化疗在HER2阳性胃食管腺癌(GEA)成人患者一线治疗中显示出具有统计学显著性和临床意义的总生存期改善。公司预计将于2026年上半年在美国和中国递交百泽安联合百赫安用于HER2阳性GEA成人患者一线治疗的新增适应症上市许可申请,并有望于2026年下半年在日本获得百泽安用于胃癌(GC)成人患者一线治疗的监管决定。不过PD-1目前作为基石疗法地位正受到PD-1/VEGF的冲击,而且全球已获批多款PD-1产品,百泽安也很难冲击K药(帕博利珠单抗)、O药(纳武利尤单抗)在全球的地位。
目前,在美国市场,百悦泽(泽布替尼,BTK抑制剂)竞争对手主要为阿斯利康的阿卡替尼和强生/艾伯维的伊布替尼(全球首个BTK抑制剂),三者销售额虽有差距,但整体而言差距不大,虽然百悦泽“头对头”对比伊布替尼临床试验中显示出更好的获益,但也很难改变三者的竞争格局。
可关注的百悦达
2026年1月6日,百济神州的百悦达(索托克拉,BCL2抑制剂)获得国家药监局附条件批准,用于治疗既往接受过至少包含布鲁顿酪氨酸激酶(BTK)抑制剂在内的一种系统治疗的慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)成人患者,以及既往接受过至少两种系统性治疗(含布鲁顿酪氨酸激酶[BTK]抑制剂)的复发或难治性套细胞淋巴瘤(MCL)成人患者。基于此次获批,索托克拉将为已接受过BTK抑制剂治疗的CLL/SLL患者带来新的治疗选择,另基于百悦泽良好的市场基础,该产品有望为百济神州带来新的增长点,不过该产品目前还未在美国、欧洲获批,百济神州管理层预计,美国食品和药品监督管理局(FDA)可能于2026年上半年决定是否批准其上市。
在2月26日、27日的两场电话会上,百济神州花了大量时间介绍索托克拉+泽布替尼组合优异的临床试验数据,其疗效胜过阿斯利康刚刚获得美国FDA批准上市的阿卡替尼+维奈克拉(BCL2抑制剂)组合,而且,百济神州认为索托克拉+泽布替尼组合将进一步帮助百济神州在CLL患者的市场拓展,百济神州总裁、全球研发负责人汪来在2月27日的电话会上解释,在整个CLL新患市场中,只有一半选择BTK单药治疗,另一半患者因为分型等原因,而选择了化疗或其他组合疗法。这部分人群才是索托克拉+泽布替尼组合的目标市场。
但整体而言,基于获批现状,索托克拉及索托克拉+泽布替尼组合市场销售还有待后续几年的检验。此外,百济神州的在研管线整体仍处于推进阶段,多款潜在药物的临床价值与商业化前景尚待临床试验结果验证。同时,业内人士分析指出,百济神州的营收高度依赖美国市场,当前复杂的地缘政治冲突,也为公司的全球业务布局带来了不确定性,可能影响其核心产品在海外市场的销售与管线推进。
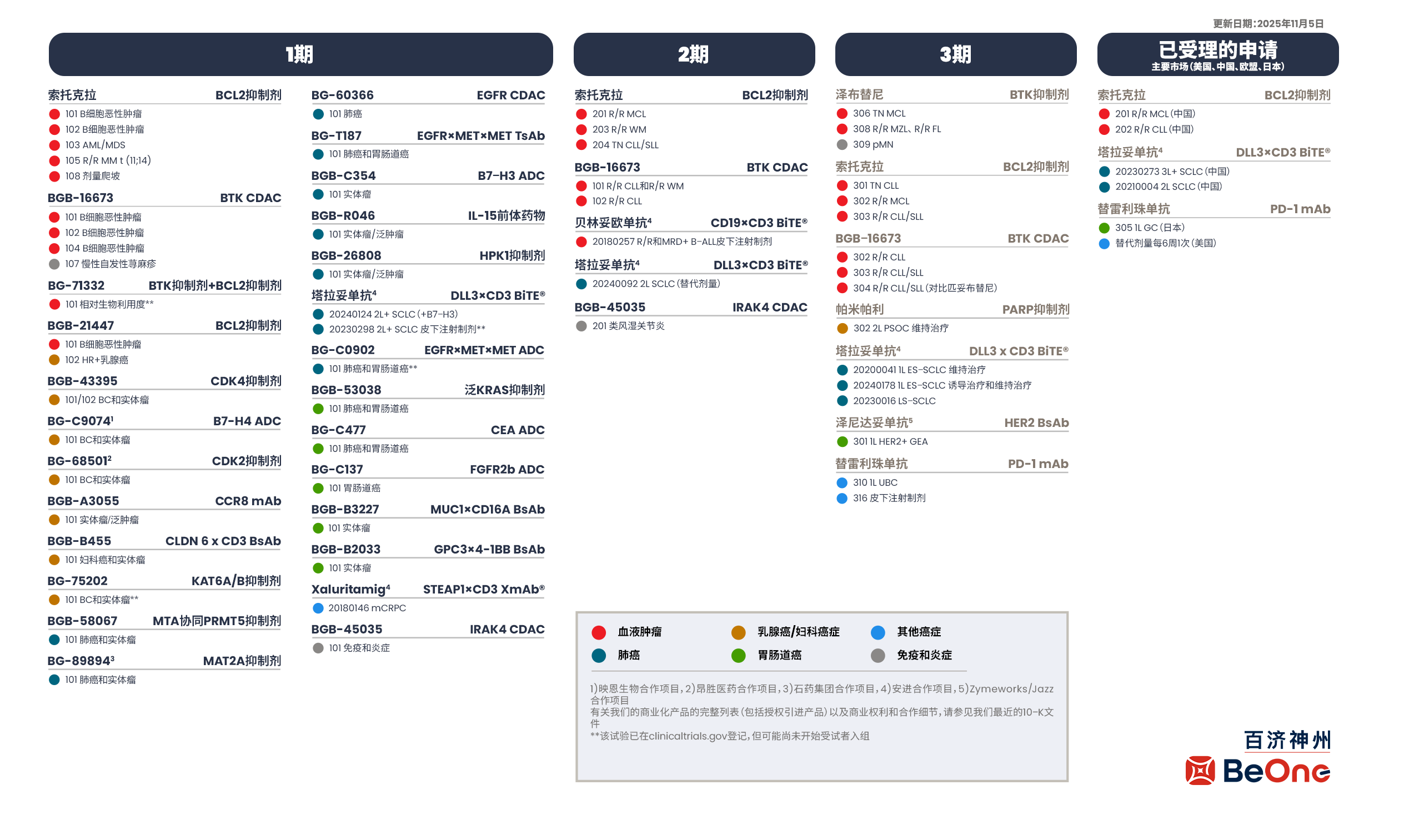
百济神州管线图 来源:百济神州官网