国内首个,恒瑞口服GLP-1/GIP双受体激动剂启动II期临床研究
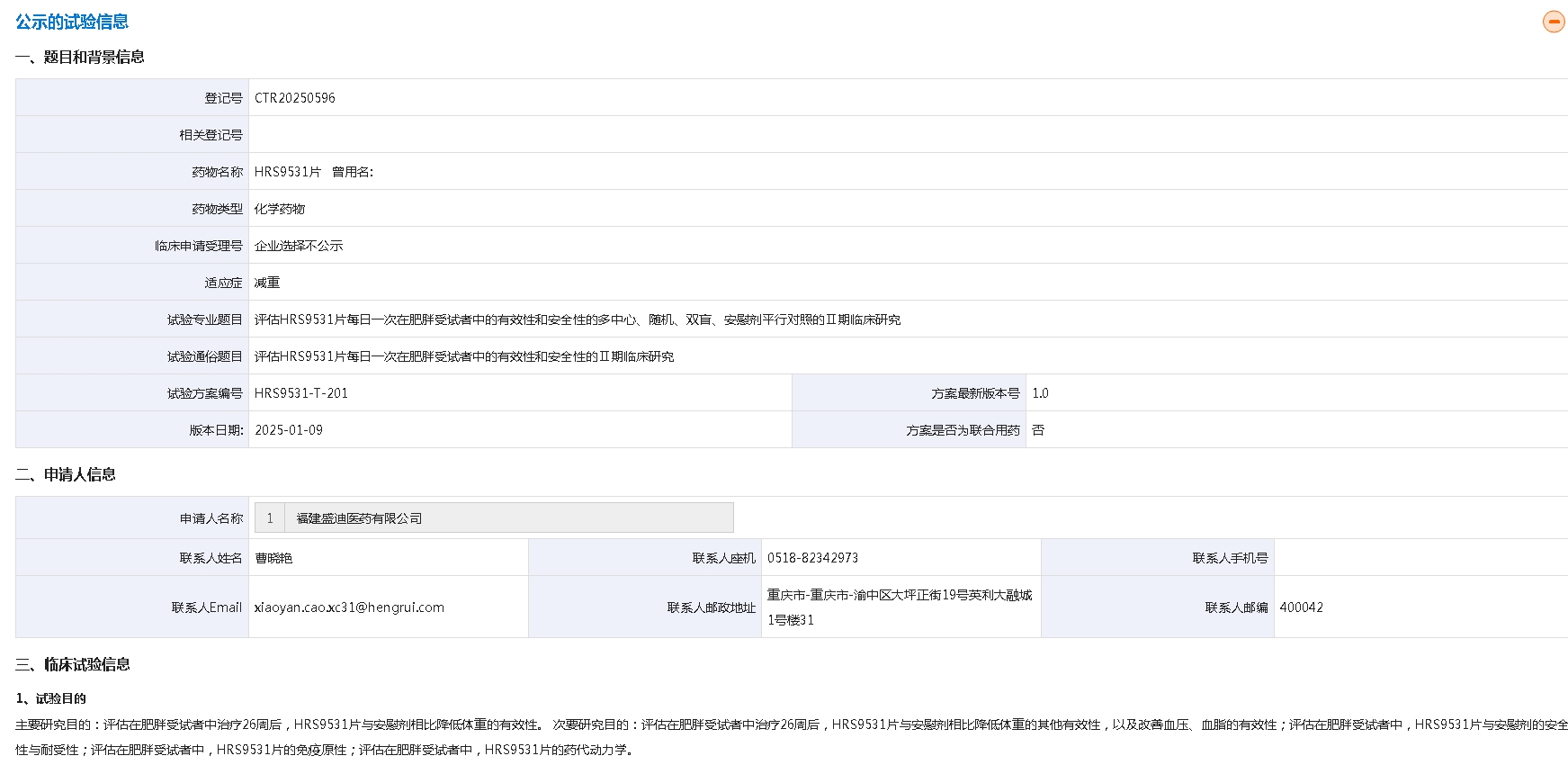
近日,据药物临床试验登记与信息公示平台显示,恒瑞医药已启动GLP-1/GIP双受体激动剂HRS9531片剂的首个II期临床研究,旨在评估每日一次服用HRS9531片在肥胖受试者中的有效性和安全性。
HRS9531注射液是由恒瑞医药自主研发的GLP-1/GIP双受体激动剂。胰高糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素多肽(GIP)是进食后由肠道合成和分泌的两种肠促胰素,它们在调节血糖和体重方面发挥着重要作用。越来越多的临床数据表明,GLP-1/GIP双受体激动剂可通过同时激动GLP-1和GIP受体产生互补或协同作用,从而减轻体重和改善血糖控制。
2024年5月,HRS9531作为恒瑞医药具有自主知识产权的GLP-1类创新药组合之一,在大中华区以外的全球范围内开发、生产和商业化的独家权利被有偿许可给了Kailera公司。通过此次合作,恒瑞医药获得的首付款加里程碑付款总额累计可高达60亿美元,并且取得了Kailera公司19.9%的股权。
目前,HRS9531有两种剂型正在针对多项适应症的进行临床开发,即注射剂和片剂。其中,HRS9531注射剂型研发进度较快,减重与降糖适应症均已进入于3期研发阶段。
在2024年美国糖尿病协会科学年会上,恒瑞医药曾披露了HRS9531注射液针对肥胖成人的Ⅱ期临床研究结果。该项随机、双盲、安慰剂对照的Ⅱ期研究旨在评估HRS9531注射液在成人无糖尿病肥胖人群中的有效性和安全性。研究共招募了249名BMI在28-40kg/m²之间的中国成年人,他们被随机分配到五个组别,分别接受每周一次的HRS9531皮下注射(剂量包括1.0mg、3.0mg、4.5mg和6.0mg)或安慰剂,持续治疗24周。主要终点是第24周时体重较基线变化的百分比。
最终的临床研究数据显示,治疗24周后,HRS9531注射液各剂量组的体重较基线均显著降低。具体来说,1.0mg、3.0mg、4.5mg和6.0mg组的体重较基线变化百分比分别为-5.4%、-13.4%、-14.0%和-16.8%,而安慰剂组仅为-0.1%。同时,治疗24周后,HRS9531注射液各剂量组体重减轻≥5%的受试者比例分别为52.0%、88.2%、92.0%和91.8%,而安慰剂组仅为10.2%。此外,HRS9531注射液还显示出改善腰围、血压、甘油三酯和血糖等代谢指标的效果,且耐受性良好,提示其在肥胖领域有巨大潜力。