新一代国产口服GLP-1药物获批临床试验
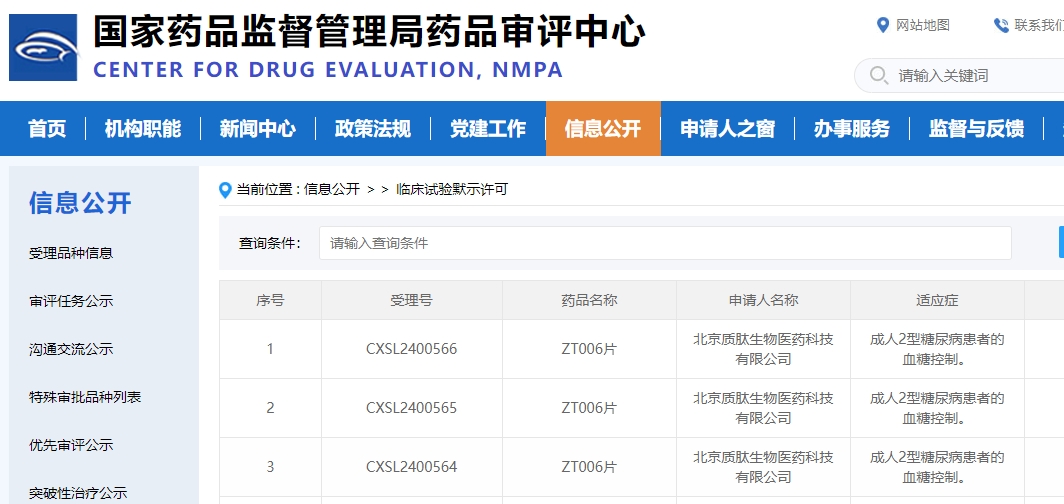
日前,根据国家药监局药审中心官网信息显示,质肽生物1类新药ZT006片获得临床试验默示许可,拟开发用于成人2型糖尿病患者的血糖控制。
根据质肽生物官网介绍,ZT006是新一代口服蛋白药品种,主要治疗糖尿病和肥胖症。经过优化的ZT006具有较高的生物利用度,有希望成为继口服司美格鲁肽之后的新一代口服GLP-1品种。口服给药是公认的、可以显著提高慢性病患者依从性的一种给药方式。
据了解,质肽生物专注于开发治疗慢性代谢性疾病(如糖尿病、肥胖、非酒精性脂肪性肝炎等)治疗领域的创新生物药,其产品管线基本围绕GLP-1靶点展开。其中,质肽生物自主研发的GLP-1注射剂ZT002已在澳洲完成一期临床研究,并于2023年分别获批在国内开展糖尿病、减重以及治疗阿尔茨海默病三项适应症的临床试验。临床实验已经证明,该分子有望实现每月一次给药。根据质肽生物方面的披露,ZT002是国内唯一进入临床的每月给药一次的GLP-1类药物。
此外,质肽生物产品管线重还有一款司美格鲁肽注射液生物类似药ZT001,目前正在围绕糖尿病和减重进行开发。2024年3月,爱美客全资子公司诺博特生物与质肽生物达成了技术授权及MAH合作协议,双方决定共同推进ZT001减重适应症在大中华地区的临床申报和产业化生产。2023年11月,爱美客参与领投了质肽生物近2亿元的B+轮融资.
今年5月,质肽生物又与通化东宝签署合作协议,根据协议约定,后者将获得前者ZT001用于治疗2型糖尿病适应症在中国大陆地区独占权益,以及共同合作开发海外市场权利。合作产品在中国大陆地区上市后,通化东宝将成为合作产品在中国大陆地区的药品上市许可持有人。目前,ZT001已在国内完成2型糖尿病适应症的临床I期,并启动了与诺和泰在2型糖尿病患者中有效性和安全性的III期临床研究。
质肽生物另一款GLP-1/FGF21双靶点激动剂ZT003则是瞄准了治疗手段几乎空白的非酒精性脂肪性肝炎(NASH),该领域潜在药物市场达到200亿美元以上。不过,该药物开发还处于早期阶段,并未进入临床试验。