迈威生物与海博生物签协商解除协议,终止两款药的合作
近日,迈威(上海)生物科技股份有限公司(以下简称“迈威生物”)及全资子公司江苏泰康生物医药有限公司(以下简称“泰康生物”)分别与扬子江药业集团有限公司(以下简称“扬子江药业”)全资子公司江苏海博生物制药有限公司(以下简称“海博生物”,曾用名:圣森生物制药有限公司,以下简称“圣森生物”)就 9MW1111(重组人源化抗 PD-1 单克隆抗体注射液)和 8MW0511(注射用重组(酵母分泌型)人血清白蛋白-人粒细胞集落刺激因子(I)融合蛋白)项目签署《协商解除协议》。
收回2款肿瘤药全部权益
资料显示,9MW1111 是一款由迈威生物自主研发的PD-1单抗,适应症为局部晚期或转移性实体瘤,截至2023年12月31日,9MW1111处于Ib期试验阶段。8MW0511 为新一代长效 G-CSF(高活性改构细胞因子),截至2023年12月31日,8MW0511新药上市申请已获得国家药品监督管理局受理,用于成年非髓性恶性肿瘤患者在接受容易引起发热性中性粒细胞减少症的骨髓抑制性抗癌药物治疗时,使用本品降低以发热性中性粒细胞减少症为表现的感染发生率。
2021年3月,迈威生物与圣森生物达成协议,圣森生物通过支付项目许可费(分首付款和里程碑付款)、销售额里程碑及售额提成的方式,独家获得前者9MW1111在中国大陆地区(不包括港澳台地区)内的开发、生产及商业化权益。圣森生物享有 9MW1111 项目与任意其他一种或多种药物的联合用药的独家开发权益。迈威生物保留开发 9MW1111 项目除单克隆抗体以外其他任意形式药物的所有权益。根据协议,圣森生物将就 9MW1111 项目向迈威生物支付项目注册里程碑费用合计 1.2 亿元及销售里程碑费用 3.5 亿元。此外,迈威生物将继续享有 9MW1111 项目商业化阶段年净销售额个位数百分比的销售提成。截至2023年12月31日,迈威生物就9MW1111项目收到扬子江药业及圣森生物支付的款项3060万元,其中2000万元为首付款,1060万元为预付研发费用。
另一款产品8MW0511的合作协议也签订于2021年3月。彼时泰康生物与圣森生物约定,圣森生物通过均摊8MW0511的研发费用、支付首付款、里程碑付款及净销售额提成的方式,独家获得8MW0511在中国大陆地区内的生产及商业化权益。根据协议,圣森生物将就8MW0511项目向迈威生物支付项目注册里程碑费用合计3亿元。此外,项目获批上市后的前5年,迈威生物负责产品生产并按照约定价格向圣森生物供货,不收取额外的收益分成。项目上市后的6-12年,圣森生物负责产品生产。6~10年,圣森生物按照净销售额的个位数百分比向公司支付销售提成;11~12年,圣森生物按照净销售额的最高10%向公司支付销售提成。
但如今,迈威生物与海博生物签协商解除协议,两款药合作终止。对于解除原因,迈威生物在公告中称,合作期内市场竞争格局变化较大,抗 PD-1 单克隆抗体产品和长效 G-CSF产品的市场价格均出现较大幅度的调整。同时公司考虑到以上两款产品均为肿瘤领域用药,未来或可与自身其他产品协同销售或开发联合疗法。据悉,8MW0511 可以广泛应用于包括肺癌、乳腺癌、尿路上皮癌、宫颈癌等各大肿瘤领域患者,与公司即将上市的适用于实体肿瘤骨转移领域及骨巨细胞瘤适应症的地舒单抗(120mg)有很好的协同效应,且针对未来上市的 ADC 产品如 9MW2821 等,可同步做好商业化体系布局,使得在产品上市后快速实现医院准入和销售增长。9MW1111 作为一款最被广泛应用的免疫疗法领域的产品,可增加未来联用 ADC的选择可能。如与 9MW2821 靶点、载荷均相同的药物 Padcev已于 2023 年 12月 15 日获 FDA 批准联合 PD-1(商品名为 Keytruda)治疗局部晚期或转移性尿路上皮癌。该联合方案在一线治疗局部晚期或转移性尿路上皮癌方面显示出超越标准治疗的优异疗效。抗 PD-1 单抗治疗恶性肿瘤的机制明确,与多款 ADC 药物联合治疗均被证实可协同增效。故经双方前期友好协商,公司收回这两个项目的全部权益。
去年营业收入1.28亿元
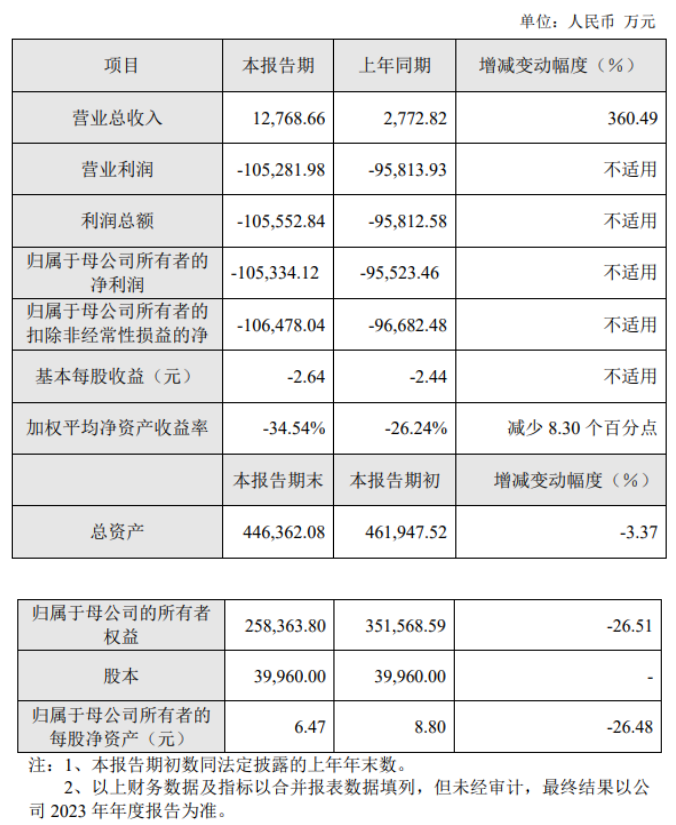
业绩快报显示,2023年度公司实现营业收入1.28亿元,同比增长360.49%;实现归母净亏损10.53亿元;基本每股亏损2.64元。
截至报告期末,迈威生物已有君迈康与迈利舒两款上市产品,均为生物类似药产品。迈威生物称,报告期内公司营业收入增长,主要系9MW3011项目与美国DISCMEDICINE,INC.(以下简称“DISC”)达成独家许可协议并收到其支付的不可退还的首付款1000万美元,同时地舒单抗生物类似药迈利舒实现新产品销售确认收入所致。该药于2023年3月底获批上市,适应症为用于骨折高风险的绝经后妇女的骨质疏松症,截至2023年末,完成发货8.45万支。
阿达木单抗生物类似药君迈康方面,该药于2022年3月获批上市,而后于2023年1月获得新增原液生产车间和生产线补充申请的批准,一季度末全面恢复商业供货。自产品恢复供应后,截至报告期末,君迈康完成发货16.69万支。
对于亏损扩大的原因,迈威生物在业绩报中称,随着新产品上市,商业化团队进一步拓展,商业化相关的销售费用例如人员薪酬及其他各类销售费用相应增加。同时,公司持续投入大量资金用于在研品种的临床试验推进,多项在研品种处于关键注册临床研究阶段导致公司研发费用金额较高。其2023年H1报显示,营业收入约8996万元,同比增加713.81%;归属于上市公司股东的净利润亏损约4.14亿元;基本每股收益亏损1.03元。