阿柏西普国内首仿获批
日前,据国家药监局官网信息显示,齐鲁制药的阿柏西普眼内注射溶液获批上市,这是国内首个获批的阿柏西普生物类似药。
阿柏西普由再生元和拜尔联合研发,是一种血管内皮生长因子(VEGF)抑制剂,能与VEGF-A和PlGF结合,从而抑制其结合和激活VEGF受体,目前主要用于新生血管(湿性)年龄相关性黄斑变性、视网膜阻塞型黄斑水肿和糖尿病性黄斑水肿。2011年,阿柏西普在美国获批上市,并于2018年正式进入中国市场。今年8月,拜耳与再生元联合推出阿柏西普8mg(每4个月给药一次)新版本也获FDA批准上市,用于治疗湿性年龄相关性黄斑变性、糖尿病性黄斑水肿和糖尿病视网膜病变患者。
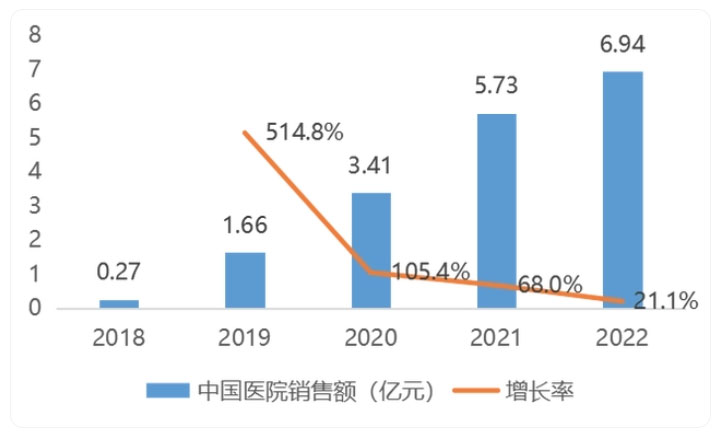
销售业绩方面,据拜耳财报,阿柏西普2022年销售额达到32.13亿欧元,同比增长10.1%,中国市场表现方面,根据药智网数据,2018-2022年,阿柏西普中国医院销售额逐年上升,2022年达6.94亿元,4年复合增长率达到了125%,预计未来仍呈增长趋势。
图片来源:药智网
另值得一提的是,原研阿柏西普专利到期时间为2025年,目前,国内也有多家企业在布局,除了齐鲁制药,还包括博安生物、迈威生物等,且已进展到临床三期阶段。