用于减重,礼来GLP-1R/GIPR双重激动剂Tirzepatide获FDA批准上市
日前,礼来宣布其葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂Tirzepatide获美国FDA批准,用于肥胖(BMI≥30 kg/m2)或至少有一种合并症(如高血压、血脂异常、2型糖尿病、阻塞性睡眠唿吸暂停或心血管疾病)的超重成人(BMI≥27 kg/m2)的长期体重管理(在低热量饮食和增加体力活动基础上)。根据礼来新闻稿,Tirzepatide成为首款获批同时激活两种肠道激素受体(GIP和GLP-1)的药物。
去年5月,Tirzepatide获得美国FDA批准,用于与控制饮食和锻炼联用,改善成人2型糖尿病患者的血糖控制。根据礼来2022年度财报业绩,Tirzepatide首年的销售业绩为4.83亿美元。业界曾认为Tirzepatide有望成为礼来继度拉糖肽后,糖尿病市场又一个王牌产品。今年第二季度,Tirzepatide则为礼来贡献了将近10亿美元的收入,该药2023年上半年销售额为15.48亿美元,礼来预计这款药物在2023年的销售额将突破40亿美元。
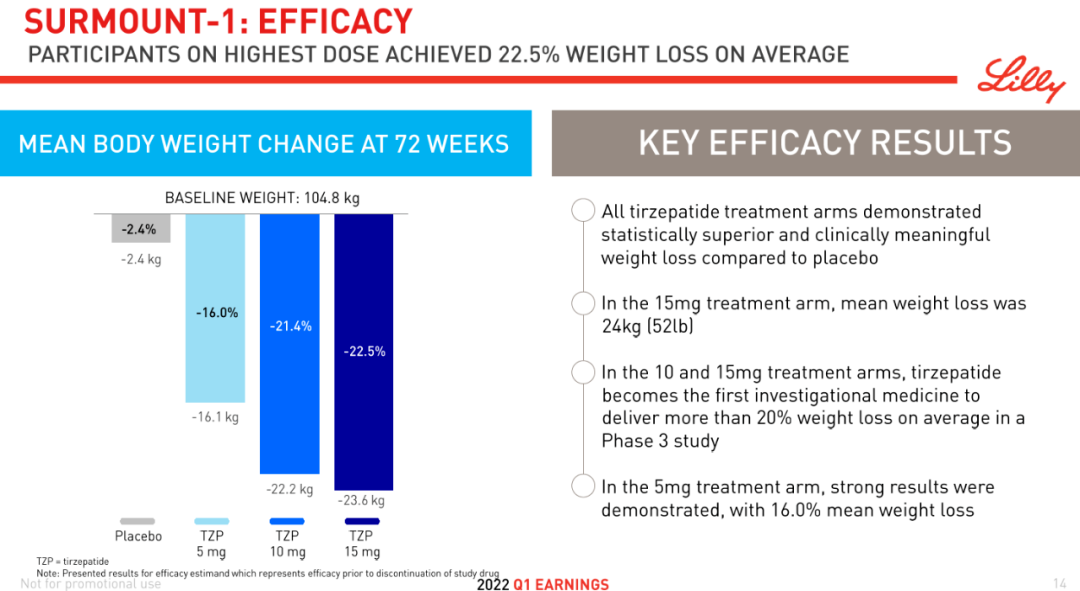
Tirzepatide获批减重适应症是基于SURMOUNT-1和SURMOUNT-2临床III期研究结果。SURMOUNT-1是一项纳入了2,539名肥胖或至少伴有一种合并症的超重的非2型糖尿病成年受试者的研究。在饮食控制和增加运动的基础上,tirzepatide受试者治疗第72周体重降低显着优于安慰剂。在15mg最高剂量组,受试者平均体重降幅可达约22公斤;在5mg最低剂量组,受试者平均体重降幅约15公斤(安慰剂组为3公斤)。
此外,根据未控制1类错误的数据,注射最高剂量tirzepatide的受试者中,有三分之一的患者体重减轻超过26公斤(体重的25%),而安慰剂组受试者体重减轻了1.5%。入组受试者的基线体重约为105公斤。
此外,在一项临床试验中,通过节食、锻炼和服用Tirzepatide来治疗肥胖或超重以及与体重相关的医疗问题的患者中观察到胆固醇的变化以及血压和腰围的减小。同时,礼来还提醒,Tirzepatide的标签包含有关甲状腺C细胞肿瘤的黑框警告。有甲状腺髓样癌个人史或家族史的患者、2型多发性内分泌肿瘤综合征患者以及已知对tirzepatide中任何赋形剂严重过敏的患者禁用Tirzepatide。
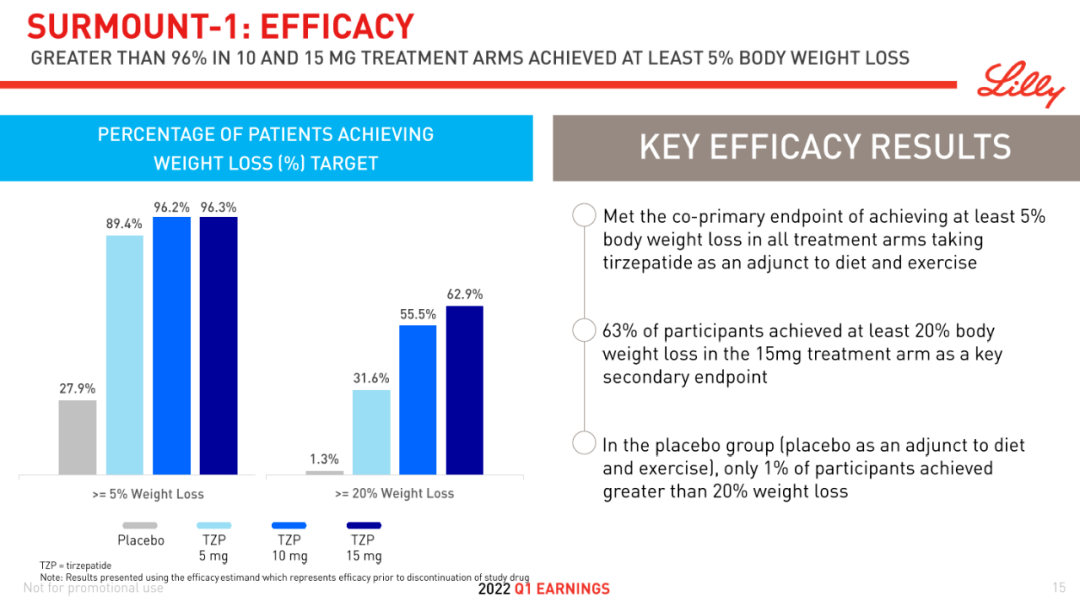
今年7月,礼来还公布了Tirzepatide在两项3期试验SURMOUNT-3和SURMOUNT-4中的积极数据。结果显示,与安慰剂相比,接受Tirzepatide治疗的患者体重平均减轻了21.1%;加上为期12周的干预期,接受Tirzepatide治疗的患者体重平均减轻了26.6%。此外,Tirzepatide组体重减轻≥5%的患者比例达94.4%,而安慰剂组这一数值仅为10.7%。
另悉,Tirzepatide将于今年年底在美国上市,共有六种剂量,一个月的供应价格约为1060美元。礼来方面称,这一价格比诺和诺德公司用于减肥的GLP-1药物Wegovy 2.4mg剂量的上市价格低约20%,诺和诺德Wegovy的价格为1,349.02美元。此外,Tirzepatide用于减重的适应症申请也已在中国提交。