华东医药“减肥针”暂停审批
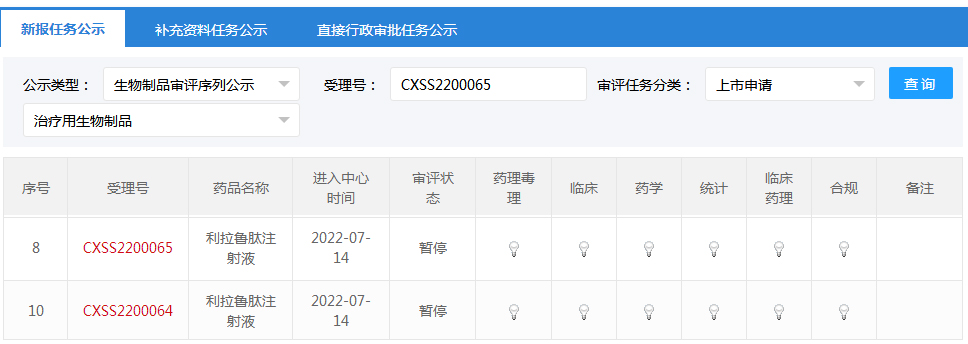
近日,据国家药监局药审中心官网信息显示,华东医药全资子公司中美华东提交的人胰高血糖素样肽-1(GLP-1)受体激动剂利拉鲁肽注射液用于肥胖或超重适应症的上市许可申请被暂停,受理号分别为CXSS2200065和CXSS2200064的上市申请状态显示为“暂停”。
据相关报道,华东医药方面对此回应称:公司利拉鲁肽注射液减肥适应症的审评因需要补充单项资料而暂停,为审评正常流程。此外,去年底的疫情对整体审评进度也有一定影响。公司预计此次暂停不会对该适应症的最终获批产生较大影响。不过,具体需要补充哪些材料,华东医药并未做更多详细说明,医谷查询华东医药相关公告信息,也暂未有消息披露。
国产第一家提出上市申请
利拉鲁肽注射液是一款GLP-1受体激动剂,也是全球第一款长效GLP-1受体激动剂,其与人GLP1具有97%的序列同源性,临床主要用于改善成年人2型糖尿病(T2DM)的血糖控制,在国外也被获批用于肥胖或体重超重患者的治疗,该药的原研企业是诺和诺德,2009年、2010年和2011年,利拉鲁肽分别获得获欧洲药品管理局(EMA)、美国FDA和原国家食品药品监督管理局批准上市(现国家药品监督管理局)的批准上市,适应症均为糖尿病,英文商品名为Victoza,中文商品名为诺和力。
2014年,利拉鲁肽用于肥胖或超重适应症获得FDA批准,商品名为Saxenda,这也是FDA批准的首个GLP-1受体激动剂用于减肥适应症,其三期临床结果显示,60%的肥胖症患者注射利拉鲁肽后体重下降5%,而三分之一患者体重的降幅能达到10%。2015年,利拉鲁肽用于减重的适应症又获得了EMA的批准,截止目前,这一适应症目前尚未在国内获批,华东医药瞅准了时机。
2022年7月,中美华东基于两项试验结果数据(暂未披露)提交了利拉鲁肽生物类似药用于减肥适应症的上市申请,为国产首家。而在这之前,中美华东还已向国家药监局提交了利拉鲁肽用于糖尿病的适应症上市许可申请。
事实上,华东医药的利拉鲁肽也并非自研,而是买来的。
2017年8月,中美华东以8000万元受让杭州九源基因工程有限公司拥有的利拉鲁肽新药技术,根据《新药技术转让合同》,中美华东成功受让利拉鲁肽新药技术并上市后的前6年里,每年需按其相关产品销售净额的3%提取并支付给杭州九源基因工程有限公司技术使用费。截至2021年12月31日,中美华东已累计支付新药技术转让款合计7200万元,加上研发投入的2.87亿元,在利拉鲁肽上已投资超3.5亿元。
有了巨额投资就更寄望于能快速实现商业化上市,所以即使产品还未上市,华东医药已在利拉鲁肽的商业布局上先行一步,2022年6月,中美华东与中东知名企业Julphar达成战略合作,授予Julphar利拉鲁肽糖尿病和减肥两个适应症在阿联酋、沙特阿拉伯、埃及、科威特、阿曼、巴林等中东和北非地区17个国家的开发、生产及商业化权益。
还在同步开发“减肥神药”司美格鲁肽
另值得关注的是,除了利拉鲁肽,华东医药还布局了另外一款GLP-1受体激动剂明星产品并被成为“减肥神药”的司美格鲁肽,根据华东医药的介绍,其目前在研发推进两款司美格鲁肽,一款由中美华东与参股公司重庆派金合作开发,分别负责临床前研究、临床研究,处于临床一期;另一款为参股公司九源基因自主研发,处于临床三期。近日,因为司美格鲁肽,华东医药“鏖战”原研企业诺和诺德引发业内关注。
这场纷争最早可追溯至2021年,当年6月,华东医药递交了司美格鲁肽的专利无效申请,2022年9月,国家知识产权局判定司美格鲁肽核心专利CN200680006674.6全部无效,理由是厂商未给出药品具体化合物的实验数据。诺和诺德日前在年报中披露,司美格鲁肽中国专利正常于2026年到期(按照该期限算,意味着国内厂商若想上市同类药品至少得等三年),针对国家知识产权局的这一决定,诺和诺德表示已上诉至北京知识产权法院,后续将进入知识产权诉讼阶段。诺和诺德如此“争锋”的背后是司美格鲁肽带给其的巨大经济效益。
据诺和诺德2022年财报业绩显示,利拉鲁肽降糖针(Victoza)、利拉鲁肽减肥针(Saxenda)分别贡献了123.22亿丹麦克朗、106.76亿丹麦克朗的销售额,而司美格鲁肽注射制剂Ozempic累计销售额达597.50亿丹麦克朗(其中在中国销售收入为21.96亿丹麦克朗),口服片剂Rybelsus销售额为112.99亿丹麦克朗,减重产品Wegovy销售额则达61.88亿丹麦克朗(同比增长346%),这也意味着仅是司美格鲁肽的系列产品就为诺和诺德贡献了合计772.37亿丹麦克朗的营收,是当之无愧的“吸金大单品”。
在中国市场,诺和诺德已提交了司美格鲁肽片(口服剂型)的上市申请并已获受理,推测申报适应症或为治疗2型糖尿病。此外,司美格鲁肽在中国开展的针对减重的一项三期临床试验已完成,业内预估,司美格鲁肽减肥适应症或将很快在华申报上市。
另悉,截止目前,国内还有多家企业在申请、开展司美格鲁肽的临床试验。其中,丽珠集团和联邦制药的同类产品进展到临床三期,与九源基因一致。