友芝友生物递表港交所,石药集团子公司为主要股东之一
12月9日,武汉友芝友生物制药股份有限公司(以下简称“友芝友”)向港交所递交招股书,拟香港主板IPO上市。
5款产品进入临床开发阶段
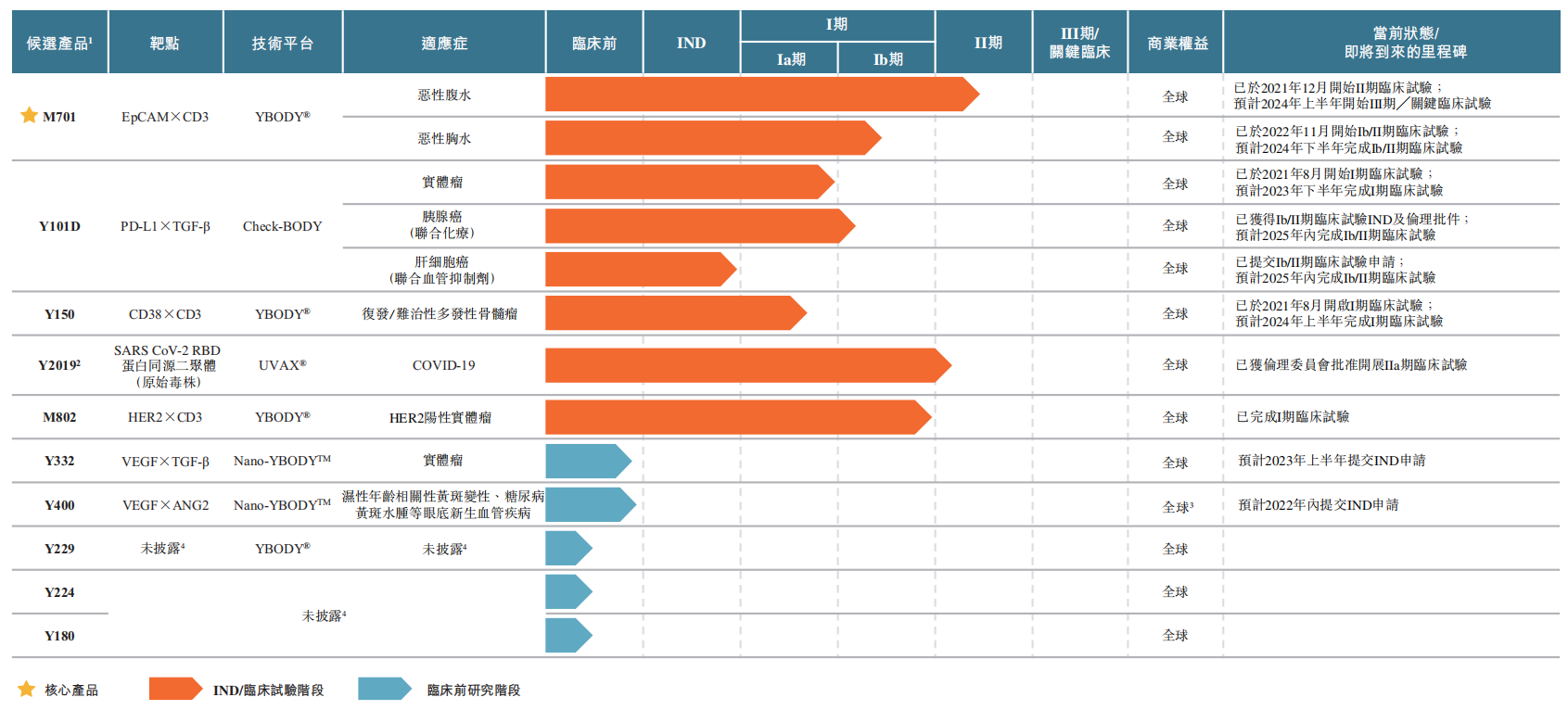
友芝友成立于2010年,专注于双特异性抗体(BsAb)靶向和肿瘤免疫疗法的开发,目前拥有四个创新平台,包括YBODY平台、Check-BODY平台、Nano-YBODY、UVAX平台。基于以上平台,友芝友目前共开发10款候选药物管线,其中5款在中国处于临床开发阶段,另外5款处于研制和临床前阶段。这些候选药主要包括:
(1)3种T细胞接合的BsAb——M701、M802和Y150
M701是一种重组BsAb,靶向EpCAM表达的癌细胞及CD3表达的T细胞,此外M701还通过抗体依赖性细胞毒性(ADCC)和补体依赖的细胞毒性(CDC)显示出对肿瘤细胞的细胞毒性。M701主要适应症为EpCAM阳性肿瘤的恶性腹水/胸水,根据弗若斯特沙利文的资料,M701是全球首款及唯一进入II期临床试验的治疗MA的EpCAM × CD3 BsAb。
M802是一种抗人表皮生长因子受体2(HER2)及抗CD3人源化BsAb,目前正在开发用于治疗HER2阳性实体瘤。在中国完成的1期临床试验数据表明,M802具有良好的安全性。根据弗若斯特沙利文的资料,M802是国内首款取得IND审批的国内自主研发BsAb。
Y150是一款重组抗CD38和抗CD3人源化BsAb,目前正处于I期临床试验中,根据弗若斯特沙利文的资料,Y150是中国唯一一款进入临床开发的靶向分化簇38(CD38)及T细胞接合的BsAb。
(2)2种靶向肿瘤微环境(TME)的候选药物——Y101D和Y332
Y101D是一种重组抗PD-L1和抗TGF-β人源化BsAb,拟用于晚期实体瘤。据悉,Y101D专门用于同时抑制PD-1/PD-L1轴和TGF-β信号通路,因此具有释放协同抗肿瘤活性和缓解耐药性的潜力。目前,Y101D正在I期临床试验中评估单药治疗转移性或局部晚期实体瘤的数据。
Y332是一款重组抗血管内皮生长因子(VEGF)及抗TGF-β BsAb,拟用于治疗多种实体瘤,目前Y332正在进行CMC研究,计划于2023年上半年向国家药监局提交IND申请。
(3)治疗老年病的靶向疗法——Y400
Y400是一款重组抗血管内皮生长因子(VEGF)和抗血管生成素-2(ANG2)的BsAb。目前Y400已完成CMC研究,预期于2022年底前向国家药监局提交IND。今年7月,友芝友与康哲药业达成关于Y400的合作,目前友芝友已收到500万美元的全额首付款。
截至最后实际可行日期,友芝友在中国拥有20项已颁发专利,在美国拥有7项已颁发专利,在其他司法权区拥有3项已颁发专利。目前,该公司还拥有47项专利申请,其中包括14项待决中国专利申请、5项待决美国专利申请。同时,根据弗若斯特沙利文的资料,在中国拥有专有双特异性平台的所有竞争对手中,友芝友的T细胞接合的BsAb在开发阶段及数量方面位列第一。
石药集团子公司为主要股东之一
资料显示,此次IPO前友芝友共完成五轮融资,包括1.57亿元A轮、1.69亿元B轮、2000万元B+轮、7350万元B++轮、2亿元C轮,C轮后估值26亿元。
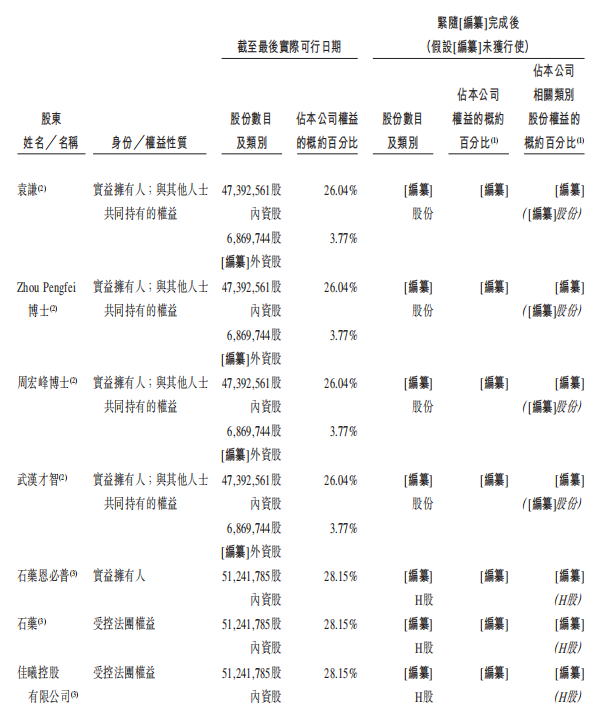
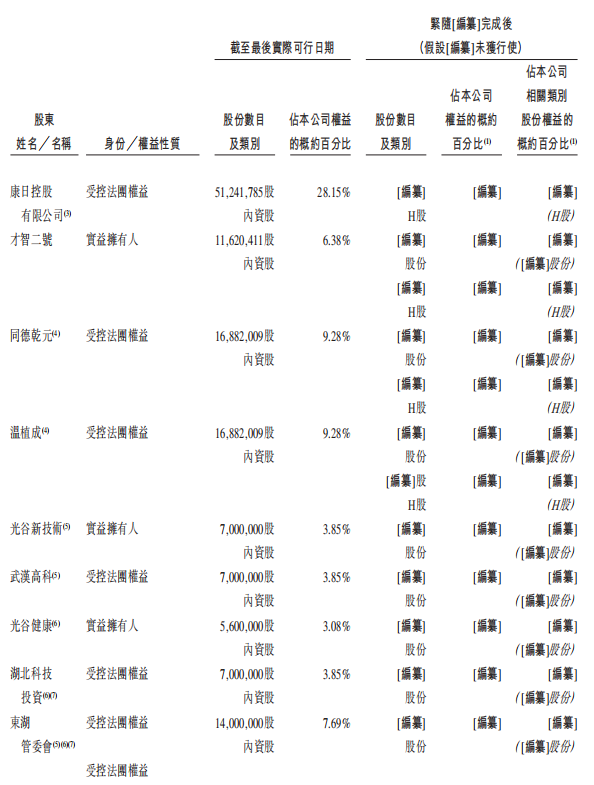
根据其招股书,本次上市前石药集团及公司石药恩必普、袁谦、武汉才智、才智二号、周宏峰、汇友兴曜、长星成长、海南博友、广瑞弘祥、光谷新技术、Zhou Pengfei和光谷健康分别持股28.15%、11.21%、9.23%、6.38%、5.60%、5.57%、4.35%、4.19%、3.95%、3.85%、3.77%和3.08%,其中石药恩必普为主要股东之一。
暂未实现商业化
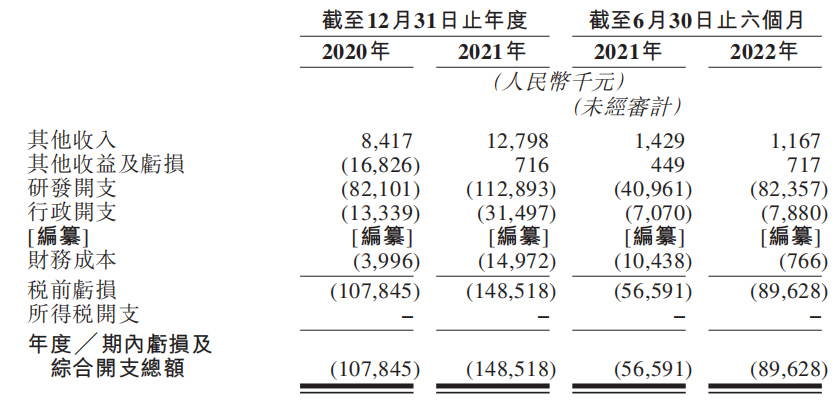
目前,友芝友尚无产品获批准进行商业销售,且没有从产品销售中产生任何收入。招股书显示,2020年、2021年和2022年上半年,友芝友的其他收入分别为841.7万元、1279.8万元和116.7万元,净亏损分别为1.08亿元、1.49亿元和8962.8万元。2020年、2021年和2021年上半年末,友芝友生物的资产总值分别为2.09亿元、2.00亿元和1.50亿元,资产净值(负债净额)分别为-3074.3万元、1.43亿元和9661.0万元,权益总额分别为-3074.3万元、1.43亿元和9661.0万元。
对于亏损,友芝友生物表示主要由研发开支、行政开支和融资成本所致。2020年、2021年及2022年上半年,友芝友的研发开支分别为8210.1万元、1.13亿元、8235.7万元。同时,
友芝友称,自成立以来已产生净亏损,并且预计于可预见未来将继续产生净亏损,且或不能产生充足收益达到或维持盈利能力,以及药品的研究、开发及商业化在所有重要方面均受到严密监管。
根据招股书,友芝友此次递表港交所,募集资金将主要用作候选药物M701、Y101D、Y150、Y2019的临床开发和商业化,推进其他候选药物(包括Y400、Y332和其他临床前候选药物)的临床前和临床研究。同时,该公司还将通过内外部投入,进一步开发和提升公司的双特异性抗体技术平台。