1年2次,长效降脂!诺华siRNA疗法国内报上市
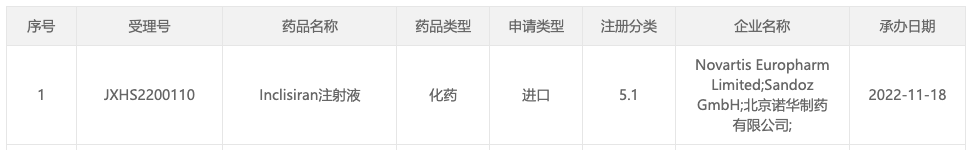
11月18日,中国国家药监局药品审评中心(CDE)官网信息显示,全球首个降低低密度脂蛋白胆固醇(LDL-C)的siRNA药物——诺华的Inclisiran注射液在国内申报上市并获得受理(受理号:JXHS2200110)。
Inclisiran是诺华以 97 亿美元收购 TMC 获得的一款靶向PCSK9的小干扰核酸(siRNA)疗法。Inclisiran可与编码PCSK9蛋白的mRNA结合,通过RNA干扰作用降低mRNA的水平、阻止肝脏产生PCSK9蛋白,从而阻止PCSK9介导的与低密度脂蛋白受体(LDLR)降解,使得血液中低密度脂蛋白的LDLR的数量增加,实现降低LDL-C水平、降低血脂的效果。
根据此前诺华披露的关键III期、安慰剂对照、双盲ORION(ORION-9、-10和-11)临床研究结果显示,对于使用最大耐受剂量的 LDL-C 降低疗法后 LDL-C 水平仍高于目标值的患者,与安慰剂组相比,接受治疗 Inclisiran 治疗的患者 LDL-C 从基线至第 510 天的平均降幅可达 50%~52% 。此外,Inclisiran在首次及第3个月初始治疗后,每年只需注射两次的给药方案有望解决患者长期依从性困境。
2020年12月,Inclisiran在欧洲获批上市,用于治疗成人原发性高胆固醇血症(杂合子家族性和非家族性)或混合型血脂异常;2021年12月该疗法在美国获批,用于治疗动脉粥样硬化性心血管疾病(ASCVD)。今年11月7日,诺华公布了为期4年的II期开放标签ORION-3扩展试验结果,该试验表明受试者LDL-C水平在4年的研究期间持续降低。
营收方面,诺华财报显示Inclisiran 在2021年的全年销售收入为1200万美元,2022年Q3销售额达到3400万美元,市场增长潜力巨大。
目前全球共有3款靶向PCSK9的药物获批上市,分别为赛诺菲/再生元的Praluent(阿利西尤单抗)和安进的Repatha(依洛尤单抗)以及诺华的Inclisiran,此外还有30多款PCSK9 抑制剂正在临床阶段。在国内,Praluent和Repatha均已获批上市,并于 2021 年纳入医保;Inclisiran则于2021年7月落地海南博鳌“乐城先行区”,并于2022年5月落地粤港澳大湾区。
目前,国内尚无国产PCSK9靶向药获批,但已有多家企业在布局,包括信达生物、君实生物、恒瑞医药、康方生物、天士力、信立泰、天广实、瑞博生物等。今年6月,信达生物宣布中国国家药品监督管理局(NMPA)正式受理由其自主研发的托莱西单抗注射液(PCSK-9单克隆抗体,研发代号:IBI306)治疗原发性高胆固醇血症(包括杂合子型家族性和非家族性高胆固醇血症)和混合型血脂异常的新药上市许可申请(NDA)。这也是首款申报上市的国产 PCSK9 单抗。