12月1日,启用《药品出口销售证明》新模板和《出口欧盟原料药证明文件》、《药品出口销售证明》电子证明
国家药监局关于启用《出口欧盟原料药证明文件》和《药品出口销售证明》电子证明的公告
(2022年第95号)
为深入贯彻落实党中央、国务院关于深化“证照分离”改革重大决策部署,优化营商环境,进一步激发市场主体发展活力,提升国家药监局“互联网+药品监管”应用服务水平,为药品出口企业提供更加高效便捷的政务服务,经研究决定,自2022年12月1日起,正式启用《出口欧盟原料药证明文件》和《药品出口销售证明》电子证明,现将有关事项公告如下:
一、 自2022年12月1日起,对签发的《出口欧盟原料药证明文件》和《药品出口销售证明》启用电子证明。电子证明与纸质证明具有同等效力。
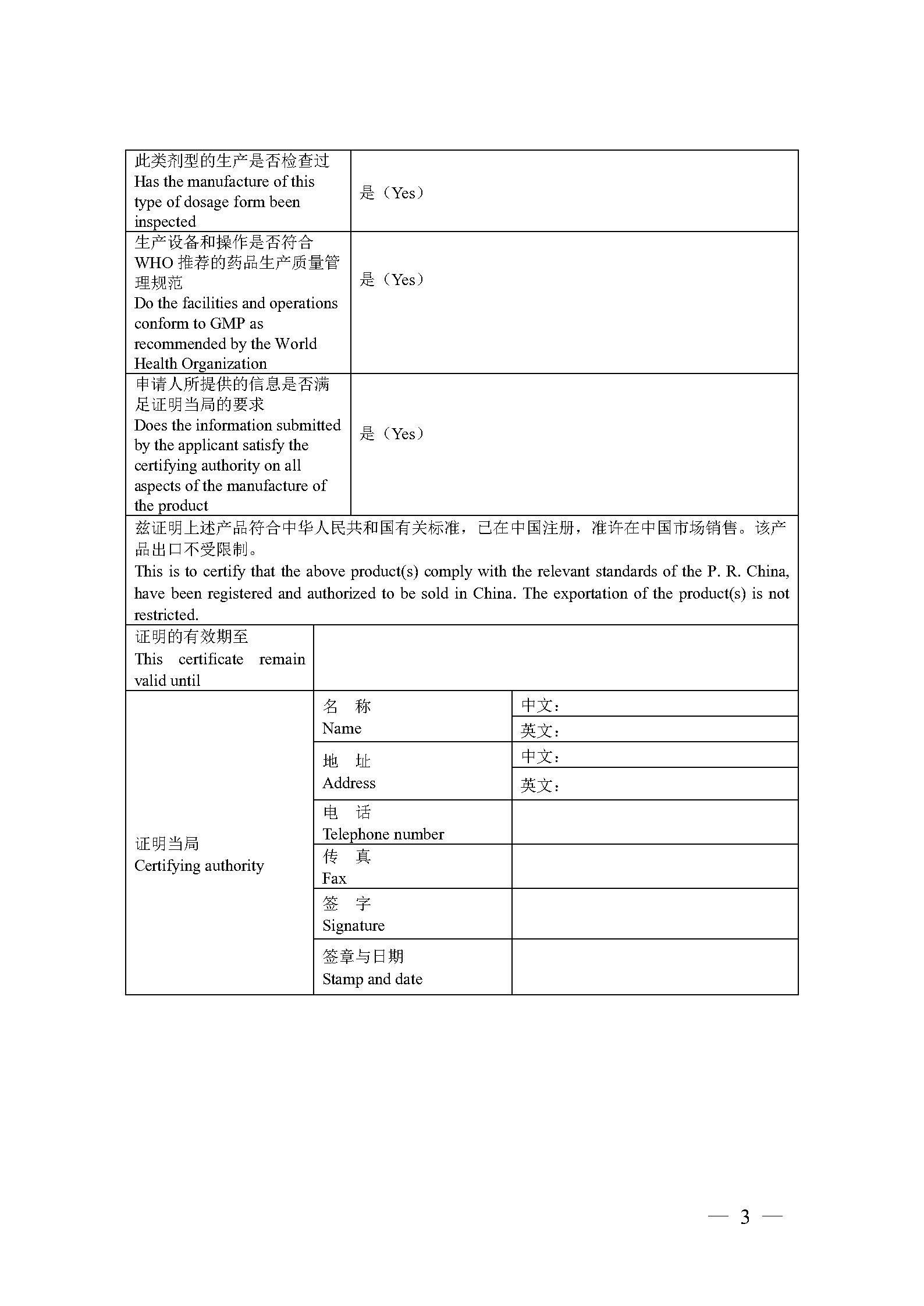
二、 结合我国药品出口工作实践和世卫组织相关最新指南,启用《药品出口销售证明》新模板(见附件)。自2022年12月1日起,各省级药品监管部门应当按照更新后的模板签发《药品出口销售证明》。
三、 做好启用电子证明的宣贯和指导工作。使用国家药监局应用系统制发的电子证明的,申请人须先行在国家药监局网上办事大厅注册并实名认证,进入网上办事大厅法人空间“我的证照”栏目,也可登录“中国药监APP”,查看下载相应的电子证明。申请人应妥善保管电子证明。国家药监局制发的电子证明常见问题及解答,见国家药监局网上办事大厅电子证照帮助栏目。
四、 使用本省应用系统制发的电子证明的,省级药品监管部门应当向行政区域内企业明确有关办事指南,做好指导和服务。
特此公告。
附件:《药品出口销售证明》模板(2022年版)
国家药监局
2022年10月27日