信迪利单抗获批第二个适应症
今日(2月3日),信达生物发布公告称,其PD-1单抗药物信迪利单抗注射液(商品名为达伯舒)联合培美曲塞和铂类化疗用于非鳞状非小细胞肺癌(nsqNSCLC)的一线治疗适应症获批,这也是继霍奇金淋巴瘤后,信迪利单抗获批的第二项适应症。
据了解,该适应症获批基于一项随机、双盲、III期对照临床研究(ORIENT-11)—信迪利单抗或安慰剂联合力比泰(注射用培美曲塞二钠)和铂类用于无EGFR敏感突变或ALK基因重排的晚期或复发性非鳞状NSCLC一线治疗,本研究随机入组397例受试者,按照2:1随机分为试验组266例,对照组131例,ORIENT-11研究证实了达伯舒?(信迪利单抗注射液)联合力比泰?(注射用培美曲塞二钠)和铂类对比安慰剂联合力比泰(注射用培美曲塞二钠)和铂类,显着延长了无进展生存期(PFS)。试验组和对照组由独立影像学评审委员会评估的中位PFS分别为8.9个月和5.0个月,HR(95%CI)=0.482(0.362,0.643),P<0.00001。期中分析时总生存期(OS)数据尚未成熟。安全性特征与既往报道的信迪利单抗研究结果一致,无新的安全性信号。
延长随访后,更新分析时试验组中位OS仍未达到,对照组中位OS为16.0个月,信迪利单抗联合化疗显着延长OS,HR(95%CI)=0.606(0.437,0.841),P=0.00250[1]。详细的OS更新数据计划于近期发表。
曾作为首个进入医保目录的PD-1产品,信迪利单抗凭借即使在此前只有一个适应症获批的情况下,也获得了不错的市场销售业绩,据信达生物日前发布的最新业绩公告显示,信迪利单抗2020年第四季度取得销售业绩达7亿元,全年销售业绩达22亿元,相比较去年10.159亿元的年销售额,整整翻了一倍多。
不过,PD-1江湖之争正在变得愈发激烈,截止目前,在6款PD-1中,获得非鳞状非小细胞肺癌一线治疗获批的还有Opvido和卡瑞利珠单抗,均为联合疗法。
同时,在最新的医保目录中,特瑞普利单抗、卡瑞利珠单抗、替雷珠丽单抗均进入医保,据相关报道称,特瑞普利单抗每瓶(规格:80mg)支付价是906.08元,替雷利珠单抗注射液每瓶(规格:100mg)支付价是1500元,卡瑞利珠单抗每瓶(规格:200mg)支付价约3000元。
再按照各家推荐的用法以及一年治疗时间估算,替雷珠丽单抗一年治疗费用或最低,费用为5.21万元;其次是特瑞普利单抗,一年治疗费用是7.07万元;最后是卡瑞利珠单抗,一年治疗费用为7.82万元。这些药品均纳入国家医保目录乙类范围,如果按照医保报销70%的比例来算,患者一年自付的费用均低于3万元,已与信迪利单抗经医保报销后年治疗费用2.9万元相差无几。而未进入医保目录的两款进口PD-1也在大幅下调治疗费用做出应对。
有业内人士表示,未来,除了价格和产能的比拼,PD-1之争更多还要在适应证拓展、海外市场开拓等方面下功夫。
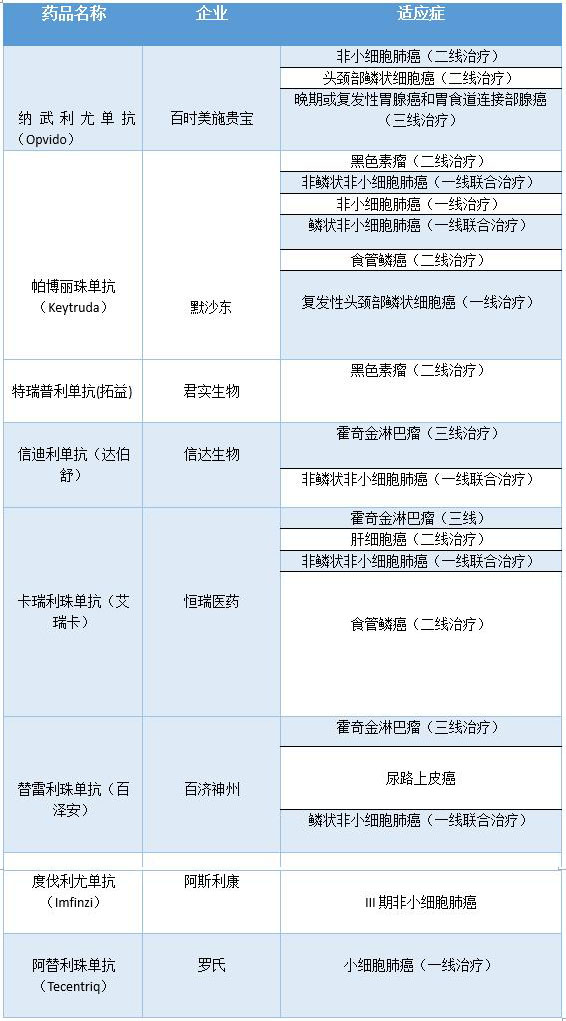
目前国内上市PD-1/PD-L1获批的适应症一览(图片来源:医谷整理)