再鼎医药今日于港交所二次上市成功
今日(9月28日),张江科学城创新型生物制药公司再鼎医药正式登陆港交所,本次发行价为562港元/股,全球发售共10,564,050股股份(未计及行使任何超额配股权),预计全球发售所得款项净额约59.4亿港元。由此,再鼎医药形成美股与港股并存上市的格局,再鼎医药也正式成为首个在香港二次上市的生物制药公司。
再鼎医药成立于2014年,通过授权引进及内部研发,目前已在肿瘤、抗感染及自体免疫三大疾病领域建立了丰富的产品管线,包括16种具有全球同类最佳/同类首创潜力的产品及候选药物,覆盖了合成致死、肿瘤电场治疗、靶向疗法、免疫肿瘤疗法、小分子、单抗及双特异性抗体等。
目前再鼎医药已有两款产品上市,分别为:
高效、选择性每日一次口服小分子聚(ADP-核糖)PARP1/2抑制剂——则乐(尼拉帕利),是目前唯一一款获FDA广泛批准用于治疗所有晚期卵巢癌患者的PARP抑制剂,已于2020年1月在中国内地正式商业上市,用于对含铂化疗完全或部分缓解的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者维持治疗。此外,今年9月8日,药监局批准了则乐的sNDA,用于对一线铂类化疗完全或部分缓解的晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌的成年患者的维持治疗。2020年上半年,则乐销售收入为1380万美元。
肿瘤电场治疗爱普盾,利用特定电场频率干扰细胞分裂,抑制肿瘤增长并使受电场影响的癌细胞死亡。2020年5月13日,再鼎医药与Novocure公司宣布,NMPA批准爱普盾的上市申请,用于与替莫唑胺联用治疗新诊断的胶质母细胞瘤患者,以及作为单一疗法用于复发胶质母细胞瘤患者。爱普盾成为15年来中国内地首个获批用GBM的疗法,今年6月爱普盾在中国内地实现商业上市。2020年上半年,爱普盾销售收入达542.2万美元。
除了上述2款产品,今年,再鼎医药的抗感染新药甲苯磺酸奥玛环素(Omadacycline)和酪氨酸激酶开关控制抑制剂瑞派替尼的中国上市申请获受理并获得了优先评审资格,即将进入收获期。其中甲苯磺酸奥玛环素用于治疗社区获得性肺炎(CABP)及急性细菌性皮肤和皮肤结构感染(ABSSSI),瑞派替尼用于治疗已接受过包括伊马替尼在内的3种及以上激酶抑制剂治疗的晚期胃肠道间质瘤(GIST)成人患者,并且已在今年7月成为海南自贸港博鳌乐城首个特批带离药物。
此外,再鼎医药的PD-1单抗注射液(INCMGA00012)于9月5日在中国获准开展临床试验,用于既往未接受过全身化疗的、不可手术的、局部复发或转移性肛管鳞状细胞癌。CD3/CD20双抗注射液(REGN1979)于9月8日在中国获批临床,用于既往全身治疗后复发或难治的B细胞非霍奇金淋巴瘤患者。
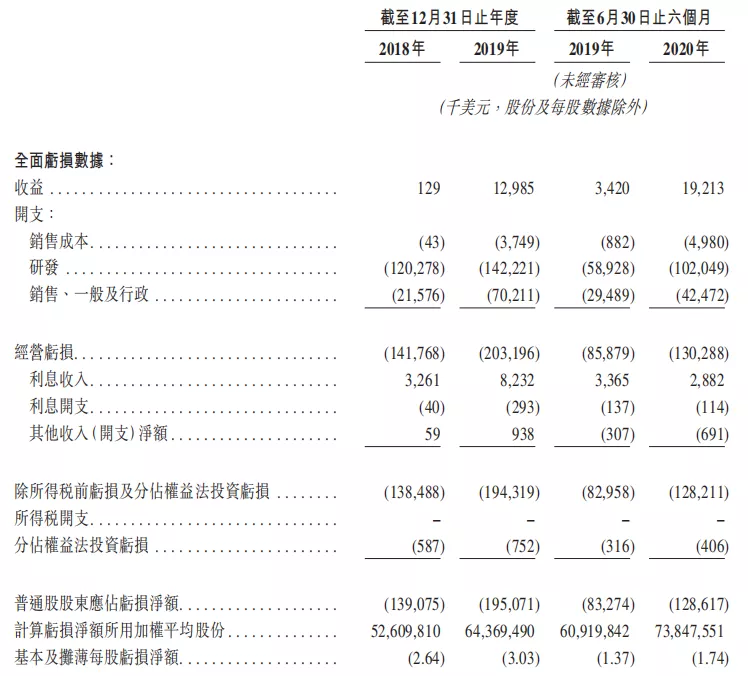
招股书披露,截至2018年及2019年12月31日止年度以及截至2020年6月30日止六个月,公司收入分别为12.9万美元、1298.5万美元及1921.3万美元,同期间的亏损净额分别为1.39亿美元、1.95亿美元及1.29亿美元。亏损净额主要来自研发开支、销售、一般及行政开支以及销售成本。再鼎医药2018年、2019年及2020年上半年研发投入分别为1.2亿美元、1.4亿元美元、1亿美元。
研发费用无疑占据大头,但随着两款产品的上市,以及多款产品的即将上市,可以预见未来再鼎医药的盈利增加。
此次在港交所上市,再鼎医药募集资金净额约57.3亿港元,并仍将重心放在了研发创新。根据规划,再鼎医药预计将所得款项净额部分,约46.2%预期用于核心产品的研发和提升商业化能力;约11.8%预期将为进行中及计划临床试验以及管线中其他候选药物(尤其是晚期候选药物)的注册申请提供资金支持,如瑞派替尼和抗HER2单克隆抗体margetuximab;约25.0%预期将用于探索新的全球授权及合作机会,并引进具有临床验证的潜在全球同类最佳/同类首创资产,7.0%用于持续投资及扩大公司的内部研发产品管线以及在全球招聘及培训高端人才;10.0%用于为营运资金及其他一般企业用途拨资。