CAR-T产品制备失败的原因及应对策略
细胞与基因治疗为肿瘤的治愈点亮了希望,但细胞与基因治疗产品的商业化制造还面临着诸多挑战。面对不同肿瘤病患复杂的样品来源,如何避免生产失败,实现高效率、标准化、规模化的生产制备,在工艺上又可以通过哪些手段或方案来满足预期的商业化需求,是大家共同关注的问题。
CAR-T产品制备失败的原因
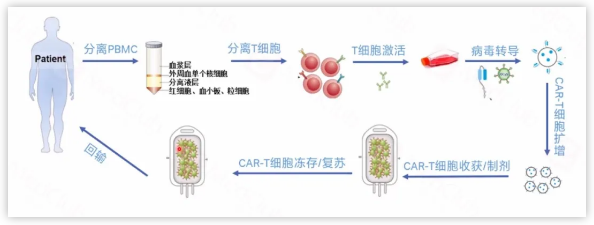
以自体CAR-T细胞制备工艺为例,从拿到病人单采血到最终收获合格的细胞产品,中间经历了细胞的分离激活,基因修饰、扩张培养、收获制剂、冻存复苏等一系列复杂耗时的工艺步骤,中间任何一个步骤出现问题,都可能导致整个生产的失败。
▲ 自体CAR-T疗法制备工艺流程
据有关文献报道,CAR-T的制备失败率高达14%。目前已经获批的诺华的Kymriah和凯特的Yescarta,在早期报道的生产失败率也基本相近,诺华Kymriah为7%-9%,凯特的Yescarta为3%-10%。主要是因为早期阶段这两家公司的工艺还有待优化,其中不少都是手工工艺。
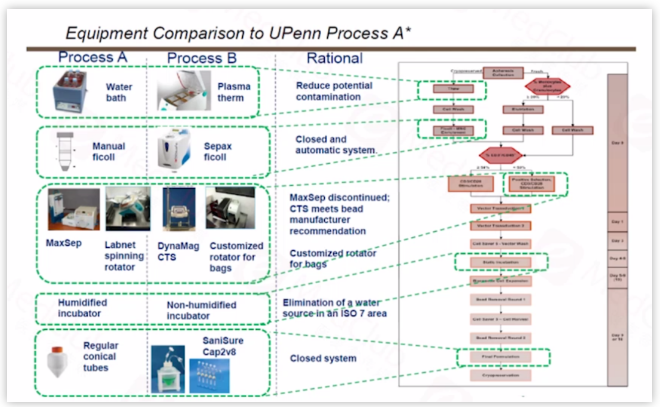
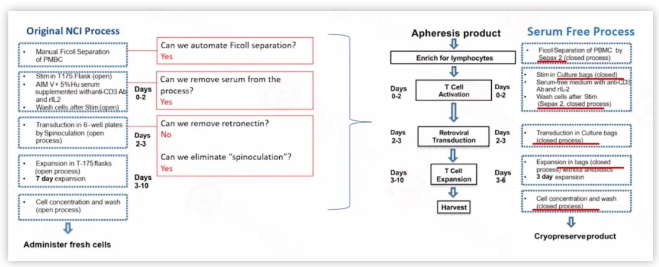
但当CAR-T产品从实验室研发到最终上市之后,这两家公司都经历了从手动到自动化的工艺转变,其中诺华将单采血样品的复苏,由传统的水浴复苏更改为污染风险小更为标准操作的干热式复苏。
单个核细胞的分离和细胞清洗步骤,也由开放式的手工法,转变为使用Sepax C-Pro系统的自动化封闭式处理方式。T细胞的培养则由静止的烘箱培养转变为封闭式的生物反应器等。整体的方向是尽量减少人为操作带来的风险,使用自动化设备来提高整体生产效率,保障产品批间的一致性,从而减少生产的失败。
凯特将单个核细胞的分离及后续工艺步骤中多个手工的细胞清洗步骤转变成封闭式的Sepax系统进行自动化的处理,而T形瓶的细胞培养方式则转变为封闭式的细胞袋的培养,来确保生产的成功,降低生产失败率。
总结诺华和凯特以及其他多家公司的经验,我们发现CAR-T细胞产品制备失败的原因主要由以下三个方面。
病人细胞个体差异:疾病导致免疫状态改变,T细胞状态及数量均不理想。
细胞产品数量不满足治疗要求。
细胞产品质量不满足治疗要求。
CAR-T产品制备失败应对策略
参考诺华和凯特的成功经验,要降低或避免细胞治疗产品制备的失败,需要从以下几个方面入手。
首先是自动化。标准化的自动化生产,能最大程度的去保障产品的一致性。同时自动化可以提高整体的生产效率,赢得病患与肿瘤抗战的宝贵时间。
其次,要保证充足数量的终产品。工艺选择时要充分考虑可以扩展的工艺,才能在商业化阶段实现规模化的生产。
而工艺的封闭性是避免产品污染和交叉污染,保障细胞产品质量的一个关键,同时也是GMP法规的重点要求。
具体优化方案
>>>> T细胞的分离
要将T细胞从成分复杂的单采血中分离出来,既要考虑分离得到尽可能多的T细胞,同时要尽可能的将粒细胞、红细胞、抗凝剂等对后续细胞生产有影响的杂质成分去掉。
在研发阶段,很多用户是使用手工的方法进行操作,耗时耗力,结果的稳定性也是差强人意。另外手工开放式操作最大的风险是污染,病人的血液样本非常宝贵,而且细胞治疗产品的终产品不能进行除菌过滤,一旦污染就完全没有拯救的余地。
>>>> 病毒转导
获得T细胞之后,如何获得稳定的传导效率和细胞活性也是相当重要的。涉及病毒的操作时,还要注意严苛地操作车间的问题,实现封闭式的病毒转染操作。
诺华和凯特以及行业内其他的主流公司都选择了Sepax C-Pro全自动封闭式细胞处理系统进行自动化的处理,解决T细胞分离和病毒转导存在的问题。Sepax C-Pro全自动封闭式细胞处理系统有着以下优势:
适用于各种来源的细胞(脐带血/骨髓/外周血/脂肪/培养细胞等)
分离/清洗/浓缩/分装以及磁珠孵育和病毒转导
高效一致的细胞回收率
封闭系统,处理安全
提高操作效率,降低操作可变性
完整可追溯性,cGMP合规
>>>> CAR-T细胞扩增
通过基因修饰获得稳定的CAR-T细胞后,还需要对它进行大规模的扩增,才能获得满足治疗要求的一个细胞量。扩增是整个工艺步骤中最耗时的极为关键的一个环节。如在最终的产品里面,效应细胞的杀伤功能和细胞活性,扩增的效率,是否能够在最短的时间内去获得大量的T细胞等,都与后续的治疗效果密切相关。
另外我们同样需要考虑避免开放式操作带来的污染风险。
综上所述,自动化封闭式的体系在细胞扩增环节非常重要,Xuri W25波浪式生物反应器是理想化的适用于细胞扩增的自动化封闭式的生物反应器。诺华、药明巨诺和行业中众多的领军企业都在使用这种工艺。Xuri W25波浪式生物反应器有以下优势:
摇动培养平台,气体及营养物质充分混匀,细胞状态更好
一次性封闭体系,无交叉污染,更安全
灌流培养实现高密度快速扩增,灵活适用不同产品管线及生产阶段
自动化远程控制,更方便
Unicorn软件实时监控记录生产过程,满足法规要求
>>>> CAR-T细胞收获/制剂
这个阶段需要将细胞里的培养基进行置换,去除细胞以外的杂质,以便符合临床回输的要求。同时要确保在这个过程中效应细胞最大程度的保留,包括细胞的数量和活性。
在研发阶段,由于细胞的体积不大,手工离心是最简单的选择,但真正到生产阶段,细胞体系可能是1L甚至更大,手工离心工作量大而繁琐,污染的风险非常高,效果得不到保障。
这个环节的解决方案是需要自动化封闭式的系统。
>>>> CAR-T细胞冻存/复苏
冻存和复苏直接关系到前期经过大量工作得到的细胞,最终回输给病人时的状态和数量,可谓临门一脚。如果在这个环节出现细胞活性变差,或者是细胞数量出现大量的损耗,甚至发生污染,就前功尽弃了。所以这个环节也非常需要稳健的工艺作为保障。
对于细胞冻存这一工艺步骤有两个非常关键的指标,分别是细胞的活性以及不被污染,精确的控速对细胞活性至关重要,所以我们需要使用可控速的程序降温仪。另外,要避免污染,就要控制可能导致污染的因素。
诺华在日本NDA阶段的Kymriah是采用这款无液氮的程序降温设备,作为从医院端采血后冻存保存的设备。
而复苏除了关注细胞的活性,也要避免解冻时对于样品的污染。传统的水浴方式,有非常高的污染风险,但采用干式的设备就能有效的避免污染的风险。诺华在Kymriah商业化生产阶段,就是选择干热式复苏设备作为水浴的替代。
Cytiva细胞与基因治疗产品是覆盖细胞与基因治疗生产全流程的,包括GMP征求意见中重点强调的信息追溯系统。
Cytiva作为生物药和细胞治疗产品生产设备的主流供应商,在细胞治疗的解决方案是由多个自动化封闭式操作方案单元组成,在满足法规对于封闭系统要求的同时,标准化的生产也极大的保障了产品的一致性,而模块化的方式,可以通过灵活的组合去适应不同的生产需求,比集成式的生产平台更为高效,也更适合细胞治疗的商业化需求。
另外结合数字化追溯系统Chronicle,还可以对细胞治疗产品生产的全过程进行科学完善的管理。
(原文有删减)