从国产新冠疫苗国内上市申请获受理看包装玻璃瓶还够用吗
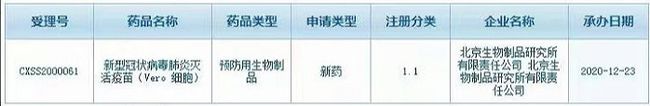
在提交上市申请一个月后,国药集团北京生物制品研究所的新型冠状病毒肺炎灭活疫苗(Vero细胞)上市申请昨日(12月23日)获得国家药监局药审中心受理。
新冠疫苗会走特殊审批通道
截止目前,国药集团疫苗已在阿联酋、巴林等国家获批上市,但并公布正式详细的三期临床试验数据,根据此前阿联酋卫生部门对国药中生提交的三期临床试验中期分析的数据进行复核,结果显示,该疫苗预防新冠感染的有效率为 86%,中和抗体转阳率为99%,预防中、重度新冠病例的有效率为100%,没有发现严重的安全隐患。
作为国内首个获得药监局受理的新冠疫苗,多长时间可以获批?
援引第一财经的报道,中国新冠疫苗的研发轨迹也是国家药审中心专家审批的轨迹,试验数据一旦出现结果,即可进入批准环节,这个速度会有多快?
“如果是按照特殊时期的审批,叫滚动式的方式,交了材料及时看,看完需补交材料的马上补充不需要再次排队,这是专对特殊时期的,如果快的话,两三天就好了。”一位药品领域专家表示。
按照《新药注册特殊审批管理规定》,特殊审批管理规定将特殊审批设置为单独通道,优先保证特殊审批新药注册申请全过程的审评审批,并按《药品注册管理办法》规定的时限完成。当存在发生突发公共卫生事件的威胁时,以及突发公共卫生事件发生后,对突发公共卫生事件应急处理所需新药按照《国家食品药品监督管理局药品特别审批程序》办理。
新冠疫苗走特殊审批通道,其批准的速度到底多快,还有待验证,但通过已有优先审批审批案例看,非特殊审批通道的HPV疫苗,在优先审批通道上,8天即获得了批准。
4月28日,国家药品监督管理局有条件批准用于预防宫颈癌的九价人乳头状瘤病毒疫苗(下称HPV疫苗)上市,距离默沙东提交申请日4月20日只过去了8天。
“从药审中心受理时间到元旦还有9天,与优先审评审批相比,特殊审批有可能会超越这个速度,不过上市条件应该还是与HPV相同,附条件上市,毕竟三期临床试验尚未结束。”一位药企负责人表示。
疫苗玻璃瓶还够用吗
国内新冠疫苗获批已进入最后的冲刺阶段,在国外已分别有辉瑞-BioNTech新冠疫苗和Moderna新冠疫苗获得紧急使用授权,这也意味着从疫苗最终走向人体,最靠前的研发端已然取得一定的成功,但疫苗的产业化或还将遭受考验。
有业内人士表示:“不要低估这里面的挑战,这需要多种不同供应链之间的协同运转,不仅是疫苗,还有玻璃瓶、橡胶塞、纸标签,如果其中任何一个环节出点问题,最终的疫苗产品都将被延迟。”
此前,上海复旦大学附属华山医院感染科主任张文宏也曾表示:疫苗的玻璃瓶的产量比疫苗还困难,玻璃瓶首先要有足够玻璃,还有足够的厂家。
有报道称,事实上,在新冠疫苗即将量产之际,装载疫苗的玻璃瓶已出现紧缺迹象。有分析机构预测,若每人接种3次,新冠疫苗全球渗透率达到20%时,需要疫苗瓶50亿支,全球渗透率达到70%时,需要疫苗瓶将近160亿支。全球范围内,几乎所有参与新冠疫苗研制的生物医药公司都在排队抢购疫苗瓶。公开资料显示,仅强生一家公司就已购买了2.5亿个疫苗瓶。全球最大的医用玻璃制造商之一肖特公司称,该公司收到的10亿个小药瓶的订货需求是其今年生产能力的两倍。
据了解,由于疫苗本身的属性,装载的玻璃瓶并不是普通的玻璃制作而成,而是硼硅玻璃,也就是加了硼和硅在里面,以增加它的抗腐蚀和抗酸碱能力,保持化学性能的稳定。
从材质和性能角度看,药用玻璃瓶主要分为两种,一种是中硼硅玻璃瓶,另一种是低硼硅玻璃瓶。
中硼硅玻璃瓶的耐水性、热稳定性、抗冷冻性等相关性更好,用于疫苗包装中可以保证疫苗质量。在欧美,法规强制要求注射用制剂、生物制剂必须使用中硼硅玻璃瓶。世界上主要的中硼硅玻璃瓶厂商是德国肖特集团、日本的NEG、美国的康宁。
与中硼硅玻璃相比,低硼硅玻璃瓶化学稳定性低,在包装PH值较高的药物时,玻璃中的碱性物质容易析出从而影响药品质量,国内主要的玻璃瓶生产商包括山东药玻、正川股份等。
但现状是我国中硼硅玻璃瓶产能存在不足,因此仍广泛使用低硼硅玻璃,我国药监局虽然在2017年的时候也提到不建议使用低硼硅玻璃和钠钙玻璃,但并没有做出硬性要求。据新浪医药报道,目前我国尚未大面积推广中硼硅玻璃的使用主要要基于两点原因:第一,中硼硅玻璃成本价格高昂,比如德国肖特公司生产的中硼硅玻璃管价格约为27000元/吨,国内低硼硅玻璃管价格约为7000元/吨,(中硼硅玻璃瓶的生产分为两步,首先是生产出中硼硅玻璃管,其次才是将玻璃管送至玻璃瓶生产商,形成最终的玻璃瓶);第二,全球中硼硅玻璃进口垄断现象严重。全球中硼硅玻璃市场长期被德国肖特、日本电气硝子和美国康宁垄断,三家公司2019年全球市占率达90%。
此前,针对药用玻璃瓶短缺,中国疫苗业协会曾回应:我国具备优质疫苗瓶生产的产业基础,疫苗玻璃瓶年产量至少达80亿支以上,能够满足新冠疫苗生产需求。有分析人士表示,事实上,这些玻璃瓶大部分都是低硼硅玻璃瓶,并不能满足新冠疫苗的包装需求。
这也意味着,如果后期国内新冠疫苗一旦获批上市实现产业化,将需要大量的中硼硅玻璃,要么自研自产,要么严重依赖进口,但由于中硼玻管的生产稳定性较难控制,山东药玻就在半年报中就表示,公司在上半年进行了中硼硅玻璃管的自主研发。在研发过程中,外观方面存在的主要缺陷是气泡线、结瘤,尺寸方面存在的缺陷主要是外径稳定性差。通过不断调整,各种缺陷有所减少,但不稳定,距离批量、稳定生产还需要一段时间。目前的模式仍是购买国外的中硼硅玻璃管,公司再制作硼硅管系列瓶和中硼硅安瓿瓶,可以看出,从国外进口实现玻璃瓶量产的可能性更大。据了解,德国肖特集团已与某全球大型医药公司已经达成合作协议并立即生效,首批药瓶将交付给中国及海外医药公司。